Les bases physico chimiques de l’eau
L’eau comment ça marche ?
De quoi est-elle composée ? Quels sont ses propriétés ? Qui ne s’est jamais posé ces questions devant son verre d’eau ?
En tout cas, moi, je me les suis posées et j’ai fini par chercher des réponses que je puisse comprendre.
L’eau est la substance la plus abondante sur Terre. Elle est présente sous trois formes :
-
liquide
-
solide (neige, glace et dans les minéraux, les hydrates naturels)
-
gazeuse
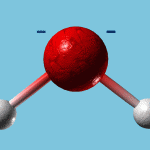
polarité de l’eau © CNRS / A. L. Siat – Ecole Estienne
Cette molécule associe deux atomes d’hydrogène (H2) et un atome d’oxygène (O). Cette molécule est dite bipolaire (ou polaire) car l’oxigène est plus électronégatif que l’hydrogène et « attire » donc les électrons des hydrogènes vers lui. L’oxygène est donc chargé négativement et les hydrogènes positivement.
Cette polarité va entraîner les liaisons entre molécules d’eau (un pôle positif attirant un pôle négatif), ces liaisons sont appelées liaisons hydrogène.
La différence entre les trois états de l’eau repose sur l’état d’exitation des molécules d’eau. Plus la température est élevée plus les molécules sont agitées et inversement.
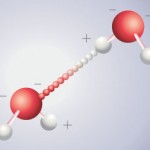
liaison hydrogène © CNRS / A. L. Siat – Ecole Estienne
Au sein de la vapeur d’eau, l’agitation est grande, les molécules se déplacent dans tous les sens, séparément les unes des autres, les liaisons hydrogène étant rendues impossibles par cette agitation.
Quand la température descend, l’agitation diminue et les liaisons hydrogène sont à nouveau possible ; les molécules s’associent en grand nombre. Les liaisons hydrogène, souples, ne durent pas longtemps et se font et se défont en permanence.
Si l’on refroidit encore la température, l’agitation thermique des molécules va diminuer et les liaisons hydrogène, qui se tordent dans l’eau liquide, vont se rigidifier pour devenir rectilignes dans la glace. Les molécules ne peuvent pas changer de position, elles ne peuvent que vibrer autour de leur position. Chaque atome d’oxygène est au centre d’un tétrahèdre dont les sommets sont occupés par les atomes d’oxygène des 4 molécules d’eau voisines. C’est là que se trouve l’explication de la glace plus légère que l’eau : la glace, du fait de ces liaisons rigides, est moins dense que l’eau liquide, elle va donc flotter sur de l’eau liquide. A volume égale, la glace prend donc plus de place que de l’eau liquide.
Et maintenant que j’ai compris ce qu’était une molécule d’eau, si j’essayais de comprendre où peut bien se nicher toute cette eau dans mon corps ?
retour au sommaire de comment ça marche


Laisser un commentaire